Atom Yarıçapı 9. Sınıf Kimya
Atom Yarıçapı
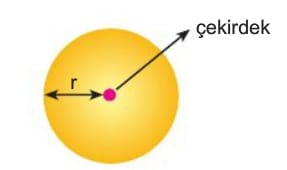
Atom yarıçapı, bir atomun çekirdeği ile çekirdeğe en uzak mesafedeki elektron arasındaki uzaklıktır.
Atom yarıçapları, elementin ya da elementin bileşiklerinin kristallerinde X-ışınlarının kırınımı yoluyla tespit edilmektedir. Bu çalışmalarda incelenen kristal yapılarında atomların dizilişlerine bağlı olarak aşağıdaki yarıçap kavramları geliştirilmiştir.
Atomun gerçekte net bir şekli yoktur. Bu nedenle atomu diğerlerinden ayırarak bir ölçüm yapılabilmesi çok güçtür.
Atom yarıçapları, elementin ya da elementin bileşiklerinin kristallerinde X-ışınlarının kırınımı yoluyla tespit edilmektedir. Bu çalışmalarda incelenen kristal yapılarında atomların dizilişlerine bağlı olarak aşağıdaki yarıçap kavramları geliştirilmiştir.
Atom Yarıçaplarının Değişimi
Periyodik sistemde aynı grupta yukarıdan aşağıya doğru inildikçe atom yarıçapı artar. Bunun nedeni her grupta, yukarıdan aşağıya doğru atomların yörünge sayısının artmasıdır.

Periyodik sistemde aynı periyotta soldan sağa doğru gidildikçe atom yarıçapı genellikle küçülür. Aynı periyotta proton sayısının artması çekirdeğin çekim gücünü de artırır. Böylece, en son yörüngedeki birim elektron başına düşen
çekim kuvveti arttığından atom yarıçapı, aynı periyotta soldan sağa doğru gidildikçe küçülür.
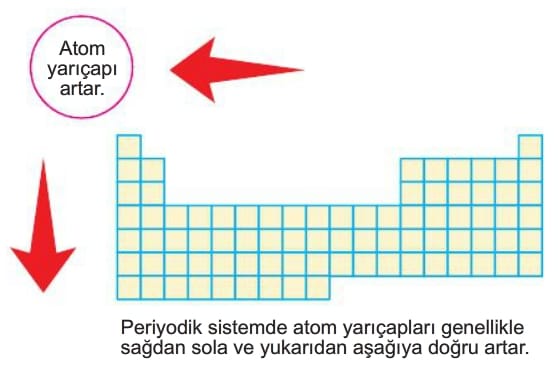
UYARI: Periyodik sistemde atom yarıçapları genellikle sağdan sola ve yukarıdan aşağıya doğru artar.
Aynı periyodun son elementi olan soy gazlar, bu eğilime uymazlar. Halojenlerden daha küçük yarıçapa sahip olması beklenen soy gazların yarıçapında büyük bir artış gözlenir. Bu değişim soy gazların van der Waals çekim kuvvetlerinin çok küçük olmasıyla açıklanabilir.
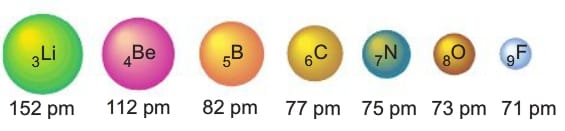
İkinci periyot elementlerinin atom çapları soldan sağa doğru küçülmektedir.
Çözümlü Örnek Sorular:
Soru 1:
Aşağıdaki elementlerden hangisinin atom yarıçapı en büyüktür?
A) Oksijen (O)
B) Sodyum (Na)
C) Klor (Cl)
D) Magnezyum (Mg)
Çözüm:
Atom yarıçapı, periyodik tabloda soldan sağa gidildikçe azalır ve yukarıdan aşağıya inildikçe artar. Bu yüzden aynı grupta altta olan elementlerin atom yarıçapı daha büyüktür. Sodyum (Na) ve magnezyum (Mg) aynı periyotta bulunur, ancak sodyum periyodik tabloda daha solda olduğu için atom yarıçapı daha büyüktür. Oksijen ve klor ise daha küçük atom yarıçapına sahiptir.
Sonuç: B) Sodyum (Na)
Soru 2:
Aşağıdaki element çiftlerinden hangisinin atom yarıçapı büyüklük sıralaması doğrudur?
A) C > O
B) Na > K
C) Cl > S
D) Mg > Al
Çözüm:
Periyodik tabloda aynı periyotta soldan sağa gidildikçe atom yarıçapı azalır, aynı grupta yukarıdan aşağıya gidildikçe artar.
- C > O: Doğru, aynı periyotta solda olan karbonun atom yarıçapı oksijenden büyüktür.
- Na > K: Yanlış, K daha büyük bir atom yarıçapına sahiptir çünkü aşağıdadır.
- Cl > S: Yanlış, kükürt klordan daha büyük atom yarıçapına sahiptir.
- Mg > Al: Yanlış, alüminyum magnezyumdan daha küçük atom yarıçapına sahiptir.
Sonuç: A) C > O
Soru 3:
Periyodik tablonun 3. periyodunda yer alan elementler için atom yarıçapı sıralaması nasıldır?
A) Na > Mg > Al > Si
B) Al > Na > Si > Mg
C) Si > Al > Mg > Na
D) Na > Si > Mg > Al
Çözüm:
Periyodik tabloda soldan sağa gidildikçe atom yarıçapı azalır. Bu durumda periyotta soldan sağa doğru atom yarıçapları küçülecektir: Na > Mg > Al > Si.
Sonuç: A) Na > Mg > Al > Si
Soru 4:
Atom yarıçapı ile ilgili aşağıdaki ifadelerden hangisi yanlıştır?
A) Aynı periyotta soldan sağa doğru atom yarıçapı azalır.
B) Aynı grupta yukarıdan aşağıya inildikçe atom yarıçapı artar.
C) Periyodik tablonun sol tarafındaki elementler daha büyük atom yarıçapına sahiptir.
D) Bir elementin atom yarıçapı, iyonlaşma enerjisi ile doğru orantılıdır.
Çözüm:
Atom yarıçapı ile iyonlaşma enerjisi ters orantılıdır. Atom yarıçapı büyük olan elementlerin iyonlaşma enerjisi daha küçüktür. Diğer ifadeler doğrudur.
Sonuç: D) Bir elementin atom yarıçapı, iyonlaşma enerjisi ile doğru orantılıdır. (Yanlıştır)
Soru 5:
Aşağıdaki elementlerin atom yarıçapı sıralaması nasıl olmalıdır?
Li, Na, K
A) Li > Na > K
B) Na > K > Li
C) K > Na > Li
D) Li > K > Na
Çözüm:
Bu elementler aynı grupta yer alır ve grupta yukarıdan aşağıya inildikçe atom yarıçapı artar. Bu durumda, sıralama K > Na > Li olacaktır.
Sonuç: C) K > Na > Li
kısa öz
çok iyi