İzotop Atomlar ve Ortalama Atom Kütlesi 10. Sınıf
Bir elementin kütle numaraları farklı olan atomlarına izotop atomlar denir. İzotoplar, aynı elementin atomları oldukları için bunların proton sayıları aynıdır. Kütle farkı, nötron sayılarının farklı olmasından kaynaklanmaktadır.
![]() proton sayıları aynı, nötron sayıları farklı olduğundan birbirlerinin izotoplarıdır.
proton sayıları aynı, nötron sayıları farklı olduğundan birbirlerinin izotoplarıdır.
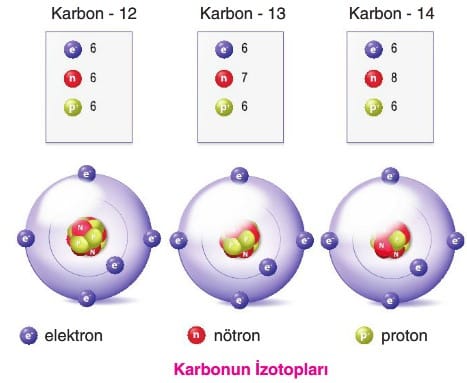
İzotopların (hem proton hem de elektron sayıları birbirine eşit olduğundan) kimyasal özellikleri aynıdır. Atom kütlelerinin farklı olmasından dolayı izotopların fiziksel özellikleri farklıdır.
İzotopları belirtmek için element adı ardından “—” işareti ve kütle numarası belirtilir: C-12, C-13 gibi.
Bir elementin izotoplarının atom kütleleri ve doğada bulunma yüzdeleri (bağıl bolluk) kütle spektrometresi adı verilen aygıtlarla belirlenir.
Doğadaki elementler iki ya da daha çok izotop atomlarının karışımı halinde bulunur. İzotopların kütlelerinin farklı olması elementin atom kütlesini de etkilemektedir. Her izotop doğada bulunuş yüzdesi oranında elementin ortalama atom kütlesini etkilediğinden elementlerin atom kütlelerinin çoğu tam sayı halinde değildir. İzotopların bulunuş yüzdeleri ise kütle spektrometresi ile ölçülmektedir. Bir elementin ortalama atom kütlesinin, o elementin doğal izotoplarının doğada bulunuş yüzdelerine bağlı olarak nasıl hesaplanacağı aşağıdaki formülde verilmiştir.
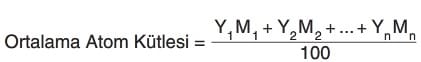

Çözümlü Örnek Test Soruları
Konu: İzotop Atomlar ve Ortalama Atom Kütlesi
1. İzotop atomlarla ilgili aşağıdaki ifadelerden hangisi doğrudur?
A) Aynı elementin farklı atomları olup, proton sayıları farklıdır.
B) Aynı elementin farklı atomları olup, nötron sayıları farklıdır.
C) Farklı elementlere ait olup, nötron sayıları aynıdır.
D) İzotop atomların kimyasal özellikleri farklıdır.
Çözüm:
İzotop atomlar, aynı elemente ait olup, proton sayıları aynıdır ancak nötron sayıları farklıdır. Proton sayısı değişmediği için kimyasal özellikleri aynıdır.
Doğru cevap: B
2. Bir elementin doğada bulunan izotoplarının yüzdeleri ve atom kütleleri aşağıda verilmiştir:
- X-30 (%70)
- X-32 (%30)
Bu elementin ortalama atom kütlesi kaçtır?
A) 30,6
B) 31,0
C) 31,4
D) 32,0
Çözüm:
Ortalama atom kütlesi şu formülle hesaplanır:
Ortalama atom kütlesi = (İzotop Kütlesi × Doğal Bolluk Yüzdesi) + (Diğer İzotop Kütlesi × Diğer Doğal Bolluk Yüzdesi)
= (30 × 0,70) + (32 × 0,30)
= 21 + 9,6 = 30,6
Doğru cevap: A
3. Aşağıdaki element çiftlerinden hangisi izotoptur?
A) ¹²₆C ve ¹⁴₇N
B) ³⁵₁₇Cl ve ³⁷₁₇Cl
C) ¹⁶₈O ve ¹⁶₇N
D) ⁴⁰₁₈Ar ve ⁴⁰₁₉K
Çözüm:
İzotop atomlar, proton sayıları aynı ancak nötron sayıları farklı olan atomlardır.
³⁵₁₇Cl ve ³⁷₁₇Cl klorun izotoplarıdır çünkü proton sayıları aynıdır.
Doğru cevap: B
4. İzotop atomlar arasında aşağıdakilerden hangisi farklıdır?
A) Proton sayısı
B) Elektron sayısı
C) Nötron sayısı
D) Kimyasal özellikleri
Çözüm:
İzotop atomlar aynı elementin farklı türleridir. Proton ve elektron sayıları aynıdır, ancak nötron sayıları farklıdır. Kimyasal özellikleri değişmez çünkü proton sayıları aynıdır.
Doğru cevap: C
5. Doğada iki farklı izotopu bulunan bir elementin ortalama atom kütlesi 35,5 olarak bulunmuştur. İzotoplarından biri 35 atom kütlesine, diğeri 37 atom kütlesine sahiptir. 35 atom kütleli izotopun doğadaki yüzdesi yaklaşık kaçtır?
A) %25
B) %50
C) %75
D) %100
Çözüm:
Ortalama atom kütlesi formülünden:
35,5 = (35 × x) + (37 × (1 – x))
35,5 = 35x + 37 – 37x
35,5 = 37 – 2x
2x = 1,5
x = 0,75 → %75
Doğru cevap: C