Doğada Karbon – Lewis Formülleri Kimya Ayt
DOĞADA KARBON — LEWİS FORMÜLLERİ
Karbonun Allotropları
Karbon organik kimyanın yapıtaşı olması nedeni ile pek çok bilimsel çalışmada yer almakta hakkında pek çok araştırmalar yapılmaktadır. Bunun sonucu olarak da karbonun doğal allotropları dışında yapay allotropları da vardır.
Elmas:
Karbonun en çok bilinen allotropudur. Mücevher olarak değerinin yanında bilinen en sert madde olduğu için kesme, delme, aşındırma işlerinde de kullanılmaktadır. Endüstriyel kullanım için doğal elmasın yanı sıra sentetik elmas da kullanılmaktadır.
Grafit
Grafit karbonun günlük hayatta sıklıkla kullandığımız doğal allotroplarındandır. Kil ile karıştırılarak kurşun kalem yapımında kullanılır. Bunun dışında kuru bir yağlayıcı olarak sanayide, tıpta vücut protezlerinin yapımında hammadde olarak ve nükleer enerji üretiminde de grafit kullanım alanı bulmaktadır.
Grafit karbonun en kararlı doğal allotropu olup elektriği iletmektedir.
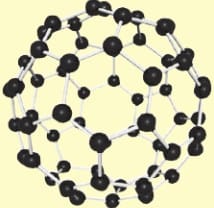
Fulleren
Fulleren karbonun yapay bir allotropudur. Üç boyutlu yapıya sahiptir. Mimar Buckminster Fuller’in tasarladığı mimari yapılara benzediği için bu isim verilmiştir. Nanoteknoloji alanından tıp alanına kadar pek çok alanda kullanılmakta olup, kullanım alanları üzerindeki çalışmalar halen devam etmektedir.
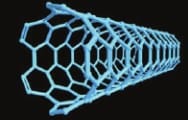
Karbon Nanotüpler
Karbon nanotüpler elektronik malzeme üretimi, optik malzeme üretimi, nanoteknoloji alanları gibi pek çok alanda kullanılan malzemelerdir. Nanotüpler fullerenler ailesinin bir üyesidir. Nanotüplerin genişliği insan saçından yaklaşık 50.000 kat daha küçüktür.
Grafen
Grafen diğer allotropların aksine iki boyutlu bir yapıya sahiptir.
Grafen ısıyı ve elektriği verimli bir şekilde iletir, manyetik özelliğe sahiptir. Grafit üretimi sırasında istenmeden çıkan bir yan üründür. İlk üretimi ve üzerinde çalışılması 2004 yılında yapılmış ve bu çalışma 2010 yılında fizik dalında Nobel ödülü almıştır. Pek çok nanoteknolojik alanda kullanım alanı bulsa da yeni bir keşif olduğu için üzerindeki çalışmalar halen devam etmektedir.
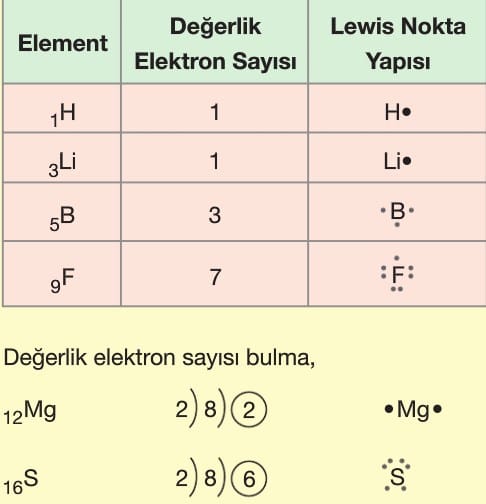
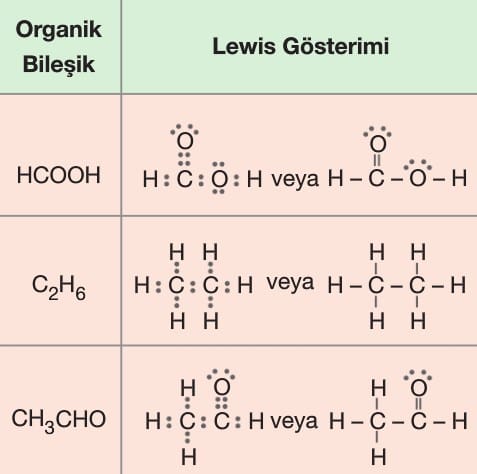
Lewis Gösterimi
A grubu elementlerinin değerlik elektronlarının, elementin sembolü etrafında nokta şeklinde gösterilmesine denir.
(Değerlik elektronları = Valens elektronları)
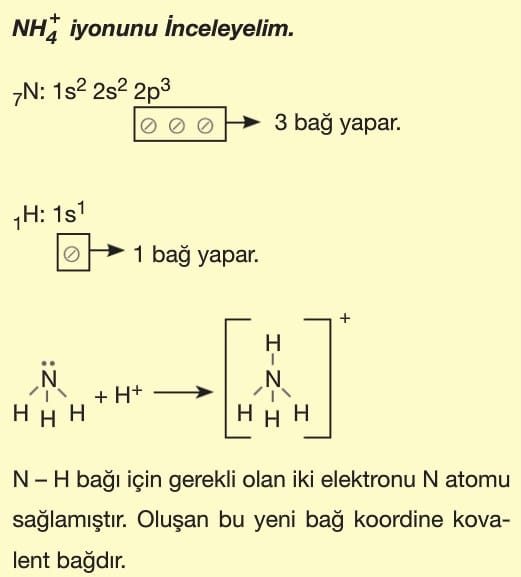
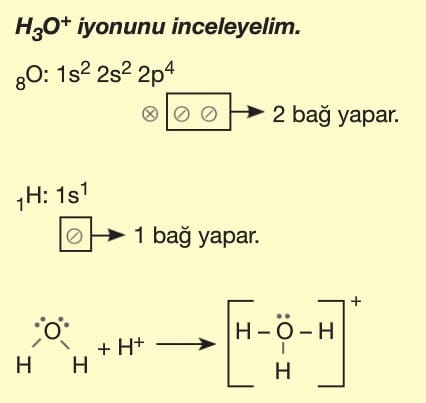
Koordine Kovalent Bağ:
İki atom arasındaki kovalent bağ oluşumunda bağın iki elektronu aynı atom tarafından sağlanıyorsa oluşan bu bağa koordine kovalent bağ denir.
Kovalent Bağ Türleri
a. Polar — Apolar Kovalent Bağ
Farklı ametal atomlarının birbirleri ile yaptığı bağlar polar kovalent bağ, aynı metal atomlarının birbirleri ile yaptığı bağlar ise apolar kovalent bağdır.
H-O Polar
C-H Polar
O-O Apolar
H- H Apolar