Dengeyi Etkileyen Faktörler 11. sınıf kimya
Denge durumunda olan bir tepkimenin sıcaklık, basınç, hacim ve madde ilavesi gibi etkiler ile denge durumu bozulabilir. Dengenin bozulacağı yönü Le Chatelier ilkesi ile tespit edebiliriz.
Le Chatelier İlkesi: Denge halindeki bir sisteme dışarıdan dengeyi bozucu bir etki yapılırsa sistem yapılan etkiyi azaltacak yönde hareket eder.
1. Derişim Etkisi
Denge anında olan bir tepkimeye tepkimede bulunan herhangi bir maddeden ilave edildiğinde (saf katı ve sıvı maddeler haricinde) denge durumundaki derişim miktarları değişecektir. Bu şekilde denge durumu bozulur. Le Chatelier ilkesine göre yeniden dengeye gelmek isteyen tepkime yapılan etkiyi en aza düşürecek şekilde ürünler ya da girenler yönünde ilerler.
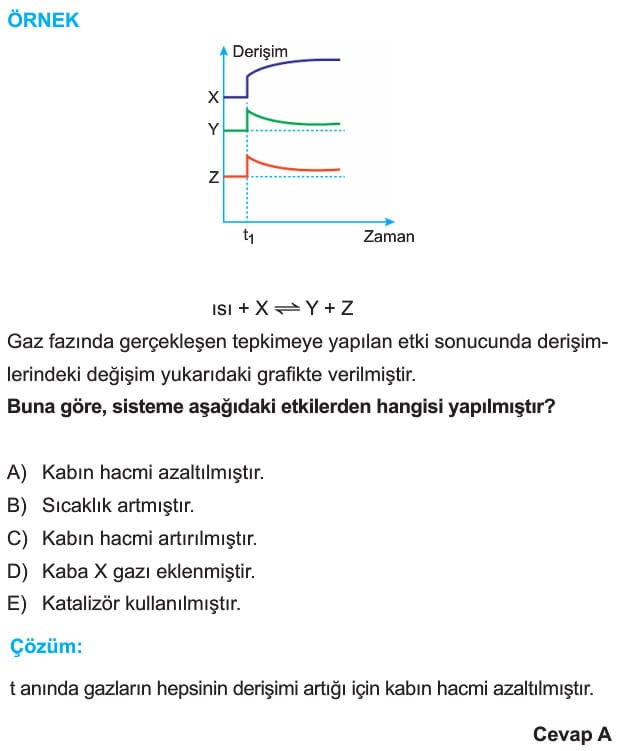
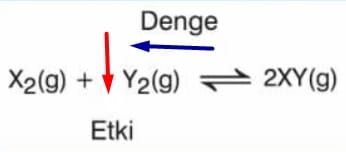
a. X2 gazı ilavesi: Dengede olan sisteme sabit sıcaklıkta X2 gazı ilave edildiğinde X2 derişimi aniden artar. Sistem bu etkiyi azaltmak üzere ürünler yönüne kayar. Zamanla X2 ve Y2 derişimi azalırken XY’nin derişimi ise artar. Ancak ilave edilen miktar baskın olduğundan başlangıca göre X2 derişimi artmış olur. Y2 derişimi azalır ve XY’nin derişimi artar.
b. XY gazı ilavesi: Dengede olan sisteme sabit sıcaklıkta XY gazı ilave edildiğinde XY derişimi aniden artar. Sistem bu etkiyi azaltmak üzere girenler yönüne kayar. Zamanla X2, Y2 ve XY’nin derişimi artar. Başlangıca göre X2, Y2 ve XY’nin derişimi artar.
c. Y2 çekilmesi: Dengede olan sistemden ortamdan sabit sıcaklıkta Y2 gazı çekildiğinde Y2 derişimi aniden azalır. Sistem bu etkiyi azaltmak üzere girenler yönüne kayar. Zamanla X2 ve Y2 derişimi artarken XY’nin derişimi azalır, Ancak çekilen miktar baskın olduğundan başlangıca göre Y2 ve XY’nin derişimi azalırken X2 artmış olur.
2. Sıcaklık Etkisi
Bir tepkimenin gerçekleştiği ortamda ortam sıcaklığı denge durumunu bozabilir. Sıcaklık etkisi denge tepkimesinin ileri yönde endotermik veya ekzotermik olmasına göre farklı etkiler yaratabilir. Sıcaklık her iki yöndeki hız sabitini değiştirebileceğinden Kc denge sabitine de etki eder.
Bilgi: Görüldüğü gibi sıcaklık etkisi denge durumunu bozduğu gibi Ki ve Kg hız sabitlerine ve Kc denge sabitine de etki etmektedir. Endotermik tepkimelerde sıcaklık artışı Kc değerini arttırırken ekzotermik tepkimelerde ise Kc değerini azaltmaktadır.
3. Hacim Etkisi
Hacim etkisi tepkimede ürün ve reaktiflerin katsayılarına bağlı olarak farklı etkilerde bulunabilir.
a. Ürün katsayılarının büyük olduğu tepkimeler de kap hacmi artarsa tüm maddelerin derişimleri ve gaz halde olanların kısmi basınçları aniden azalır (saf katı ve sıvılar hariç) Tepkime yeniden dengeye gelebilmek için azalan derişim ve kısmi basınç değerlerini arttırmak üzere gaz fazındaki katsayının büyük olduğu (ürünler) tarafa kayar.
b. Giren katsayılarının büyük olduğu tepkimeler de kap hacmi artarsa tüm maddelerin derişimleri ve gaz halde olanların kısmi basınçları aniden azalır (saf katı ve sıvılar hariç). Tepkime yeniden dengeye gelebilmek için azalan derişim ve kısmi basınç değerlerini arttırmak üzere gaz fazındaki katsayının büyük olduğu (girenler) tarafına kayar.
c. Giren ve ürünlerin katsayılarının eşit olduğu tepkimeler de kap hacmi artarsa tüm maddelerin derişimleri ve gaz halde olanların kısmi basınçları aniden azalır (saf katı ve sıvılar hariç). Ancak denge durumu bozulmaz. Ancak başlangıca göre derişim ve kısmi basınç azalır.
Dengeyi Etkileyen Faktörler Soruları ve Çözümleri
Çözümlü Örnek Test Soruları
Dengeyi Etkileyen Faktörler
Le Chatelier prensibine göre, kimyasal denge bir dış etkiyle bozulduğunda sistem bu etkiye karşı koymak için kendini yeniden dengeye getirir. Dengeyi etkileyen faktörler arasında sıcaklık, basınç, derişim değişiklikleri ve katalizör kullanımı bulunur.
1. Bir denge tepkimesinde basınç artırıldığında hangi koşulda sistem dengeyi sağlamak için ileri yönde kayar?
A) Reaksiyonda toplam gaz molekülü sayısı azalırsa.
B) Reaksiyonda toplam gaz molekülü sayısı artarsa.
C) Basınç değişimi dengeyi etkilemez.
D) Sadece katalizör varsa denge etkilenir.
Çözüm: Basınç arttığında, denge daha az gaz molekülü içeren tarafa kayar. Bu, basıncın azaltılmasına yönelik bir tepkidir. Cevap A.
2. Aşağıdaki tepkimelerden hangisinde sıcaklığın artırılması dengeyi ürünler yönüne kaydırır?
A) N₂(g) + 3 H₂(g) ⇌ 2 NH₃(g) (Ekzotermik)
B) 2 SO₂(g) + O₂(g) ⇌ 2 SO₃(g) (Ekzotermik)
C) H₂O(g) ⇌ H₂(g) + ½ O₂(g) (Endotermik)
D) CH₄(g) + 2 O₂(g) ⇌ CO₂(g) + 2 H₂O(g) (Ekzotermik)
Çözüm: Sıcaklık arttığında endotermik tepkimeler ileri yönde gerçekleşir. Bu nedenle endotermik olan H₂O(g) ⇌ H₂(g) + ½ O₂(g) tepkimesi ürünler yönüne kayar. Cevap C.
3. SO₂(g) + O₂(g) ⇌ 2 SO₃(g) tepkimesinde O₂ derişimi artırılırsa denge nasıl etkilenir?
A) Denge reaktanlar yönüne kayar.
B) Denge ürünler yönüne kayar.
C) Tepkime hızı azalır.
D) Denge değişmez.
Çözüm: O₂ derişiminin artırılması, dengeyi ürünler yönüne kaydırır. Cevap B.
4. Aşağıdaki denge tepkimelerinden hangisinde basınç artırıldığında denge reaktanlar yönüne kayar?
A) 2 H₂(g) + O₂(g) ⇌ 2 H₂O(g)
B) N₂(g) + 3 H₂(g) ⇌ 2 NH₃(g)
C) CO(g) + 3 H₂(g) ⇌ CH₄(g) + H₂O(g)
D) 2 NO(g) ⇌ N₂(g) + O₂(g)
Çözüm: Basınç artırıldığında denge, gaz molekülü sayısının fazla olduğu tarafa kaymaz. Bu nedenle, D şıkkındaki tepkimede denge reaktanlar yönüne kayar. Cevap D.
5. Tepkime sıcaklığının artırılması aşağıdaki denge tepkimelerinden hangisinde dengeyi reaktanlar yönüne kaydırır?
A) C + O₂ ⇌ CO₂ (Ekzotermik)
B) CaCO₃ ⇌ CaO + CO₂ (Endotermik)
C) N₂ + 3 H₂ ⇌ 2 NH₃ (Ekzotermik)
D) CH₄ + H₂O ⇌ CO + 3 H₂ (Endotermik)
Çözüm: Sıcaklık artırıldığında ekzotermik tepkimelerde denge reaktanlar yönüne kayar. Bu nedenle C şıkkındaki tepkime geri yönüne kayacaktır. Cevap C.
6. Le Chatelier prensibine göre, bir tepkimede katalizör eklendiğinde denge nasıl değişir?
A) Denge katalizör eklenince bozulur.
B) Denge ürünler yönüne kayar.
C) Denge reaktanlar yönüne kayar.
D) Katalizör dengeyi etkilemez, sadece tepkime hızını artırır.
Çözüm: Katalizörler, dengeyi değiştirmez, sadece tepkime hızını artırır. Cevap D.