Çözünürlük 11. sınıf kimya
Testler ve Çalışma Kağıdı mı Lazım?
İstediğin konuyu yaz; MEB uyumlu çoktan seçmeli testler, konu özetleri ve çalışma kağıtları saniyeler içinde hazırlansın. Ücretsiz PDF indir!
Öncelikle çözünme olayının nasıl gerçekleştiğini hatırlayalım. İki madde birbiri içerisinde karıştırıldığında madde türlerine bağlı olarak aralarında etkileşimler görülür. Bu etkileşim sonucunda maddelerden biri diğeri içerinde tamamen dağılıyor ise çözünme gerçekleşir. Örneğin NaCl(k) tuzu suya atıldığında Na+ iyonları sudaki oksijen tarafından sarılırken Cl– iyonları da sudaki hidrojenler tarafından sarılır.
Çözünürlük: Sabit sıcaklık ve basınçta 100 g (cm3, mL) suda çözünebilen en fazla madde miktarına çözünürlük denir. Çözünürlük g/100 g su şeklinde gösterilir.
Çözelti: Homojen karışımdır. Şekerli su, alkollü su, doğal gaz çözeltilere örnek verilebilir.
Çözeltilerin Sınıflandırılması
1. Çözünürlüğe Göre Çözelti Türleri
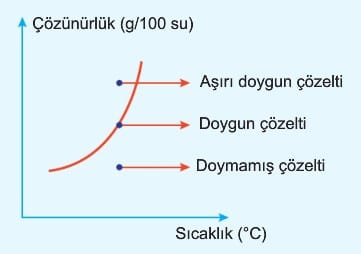
a. Doymamış Çözelti: Belirli sıcaklık ve basınçta bir miktar suyun çözebileceğinden daha az madde çözmüş olduğu çözeltilere denir.
b. Doymuş çözelti: Belirli sıcaklık ve basınçta bir miktar suyun çözebileceği kadar maddeyi çözmüş olduğu çözeltilere denir.
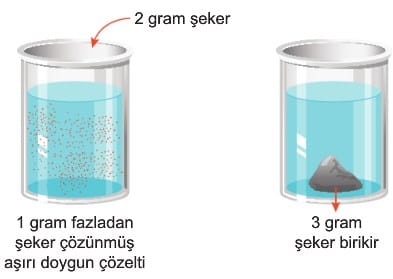
c. Aşırı doymuş çözelti: Öncelikle belirli sıcaklıkta doygun çözelti hazırlanır. Çözünme ısı alarak gerçekleşiyor ise bu çözelti uygun bir şekilde soğutularak çözünen maddenin bir kısmı çökmesi gerekirken çözücü içinde askıda kalır. Ancak bu durum kararsızdır. Yapılan etki ile fazlalık madde dibe çöker ve çözelti doygun hale gelir. Örneğin 1 gram fazla şeker çözünerek hazırlanan çözeltiye 2 gram şeker eklendiğinde kabın dibinde 3 gram şeker oluşur. Dipte biriken şeker eklenen şeker değildir. Eklenen şeker çözünürken çözeltinin alt kısmındaki şeker tanecikleri birleşerek kabın dibine çöker.
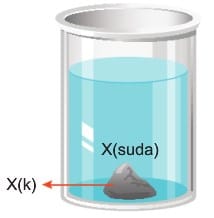
Dibinde katısı bulunan çözeltiler doygundur. Aşırı doygun değildir. Bu çözeltilerde çözünme ve çökelme olayları aynı hızla devam etmektedir.
2. çözünen Miktarına Göre Çözelti Türleri
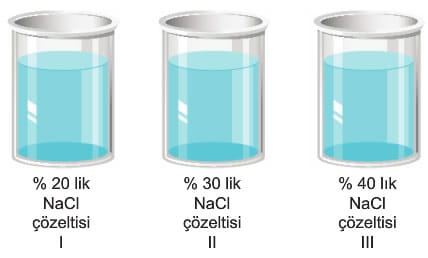
Bu tür çözeltilerde bir çözeltiye bakılarak karar verilmez. Mutlaka aynı maddenin başka bir çözeltisi ile kıyaslanmalıdır. Karşılaştırılan çözeltilerden derişimi az olan diğerine göre seyreltik, derişimi fazla olan da diğerine göre derişiktir. Çözeltilerin seyreltik veya derişik olmasının doygunluk ile ilgisi yoktur. Bir çözelti doygundur ancak farklı bir sıcaklıktaki doymamış bir çözeltiden daha seyreltik olabilir.
3. Elektrik İletkenliğine Göre Çözelti Türleri
Suda çözündüğünde iyonlarına ayrışan veya iyon oluşturan maddelerin sulu çözeltileri elektrik akımını iletir. Bu çözeltilere elektrolit çözelti denir. Çözelti içerisindeki iyon derişimi ve çözeltinin sıcaklığı artıkça elektrik iletkenliği artar. Bu çözeltilerde elektrik iletkenliği iyon hareketi ile sağlanır. Elektrik akımını iletmeyen çözeltilere ise elektrolit olmayan çözelti denir.
Bilgi: Çözeltilerin elektriği iletmesi sırasında kimyasal olay gerçekleşir. Bu tepkimelere elektroliz tepkimesi denir. Bu konuyu 12. sınıf elektrokimya konusunda öğreneceksiniz. Metallerin elektriği iletmesi fizikseldir ve elektrik akımı elektron hareketi ile taşınır.
Çözümlü Örnek Test Soruları
Çözünürlük
Bir maddenin belirli bir sıcaklık ve basınç altında bir çözücüde ne kadar çözünebileceği çözünürlük ile tanımlanır. Çözünürlük, maddenin kimyasal özelliklerine ve ortamın koşullarına bağlı olarak değişir.
1. Bir tuzun su içerisinde çözünürlüğü 30°C’de 20 g/100 mL iken, 40°C’de 30 g/100 mL’ye çıkmaktadır. Bu gözleme dayanarak çözünürlükle ilgili aşağıdakilerden hangisi doğrudur?
A) Sıcaklık arttıkça çözünürlük azalır.
B) Tuzun çözünürlüğü sıcaklıkla birlikte artmaktadır.
C) Tuzun çözünürlüğü sıcaklıktan bağımsızdır.
D) Çözünürlük yalnızca çözücü türüne bağlıdır.
Çözüm: Verilen bilgilere göre, sıcaklık arttıkça tuzun çözünürlüğü artmaktadır. Bu, çözünürlükle sıcaklık arasındaki ilişkiye dayanır. Cevap B.
2. Aşağıdaki çözeltilerden hangisi doygun bir çözelti tanımına uyar?
A) Çözünen miktarının çözebileceğinden daha fazla olduğu çözelti.
B) Çözünenin tamamen çözündüğü ve çözünmenin durduğu çözelti.
C) Çözücünün çözünen maddeden daha fazla olduğu çözelti.
D) Çözünen maddenin çözünürlüğünden daha az madde içerdiği çözelti.
Çözüm: Doygun bir çözelti, çözücü belirli bir sıcaklıkta çözünebileceği kadar çözünen maddeyi içerdiğinde oluşur. Bu durumda çözünen artık çözünemez ve denge sağlanır. Cevap B.
3. Aşağıdakilerden hangisi bir gazın su içerisindeki çözünürlüğünü etkileyen faktörlerden biri değildir?
A) Sıcaklık
B) Basınç
C) Çözücünün türü
D) Gazın moleküler kütlesi
Çözüm: Bir gazın çözünürlüğü sıcaklık ve basınç gibi faktörlere bağlıdır. Ancak gazın moleküler kütlesi çözünürlüğü doğrudan etkilemez. Cevap D.
4. Bir katı madde sıcak suya ekleniyor ve çözülme süreci hızlanıyor. Bu durumda aşağıdakilerden hangisi çözünürlüğü artıran faktörlerden biridir?
A) Sıcaklık artışı
B) Basınç artışı
C) Çözücünün hacminin azaltılması
D) Çözünenin miktarının artırılması
Çözüm: Katı maddelerin çözünürlüğü genellikle sıcaklık arttıkça artar. Bu nedenle sıcaklık artışı çözünürlüğü artıran önemli bir faktördür. Cevap A.
5. Doymamış bir çözeltide çözünürlük sınırına ulaşılmadan daha fazla çözünen eklenirse ne olur?
A) Çözünen çözülmeye devam eder.
B) Çözünen madde dibe çöker.
C) Çözelti doygun hale gelir ve çözünme durur.
D) Çözünen çözeltinin rengini değiştirir.
Çözüm: Doymamış bir çözeltide, çözücü hala daha fazla çözünen maddeyi çözebilir. Bu durumda çözünen çözülmeye devam eder. Cevap A.
6. Sıcaklığın çözünürlüğe etkisiyle ilgili olarak aşağıdaki maddelerden hangisi genellikle daha az çözünür hale gelir?
A) Katılar
B) Sıvılar
C) Gazlar
D) İyonik bileşikler
Çözüm: Gazların çözünürlüğü sıcaklık arttıkça genellikle azalır. Cevap C.