Çözünürlüğe Etki Eden Faktörler 11. sınıf kimya
Çözünmeye etki eden faktörleri;
- Çözücü ve çözünenin türü
- Sıcaklık
- Basınç
- Ortak iyon derişimi
olarak sıralayabiliriz.
1. Çözücü ve Çözünen Türü
Polar yapılı maddeler polar çözücülerde, apolar yapılı maddeler apolar çözücülerde daha iyi çözünür. Polar yapılı olan NH3 ve HCl molekülleri polar olan suda iyi çözünür.
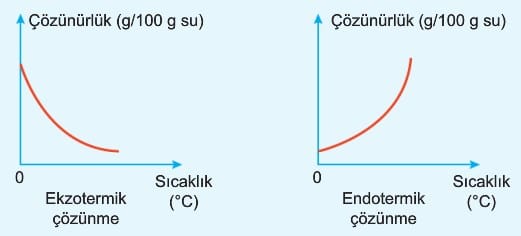
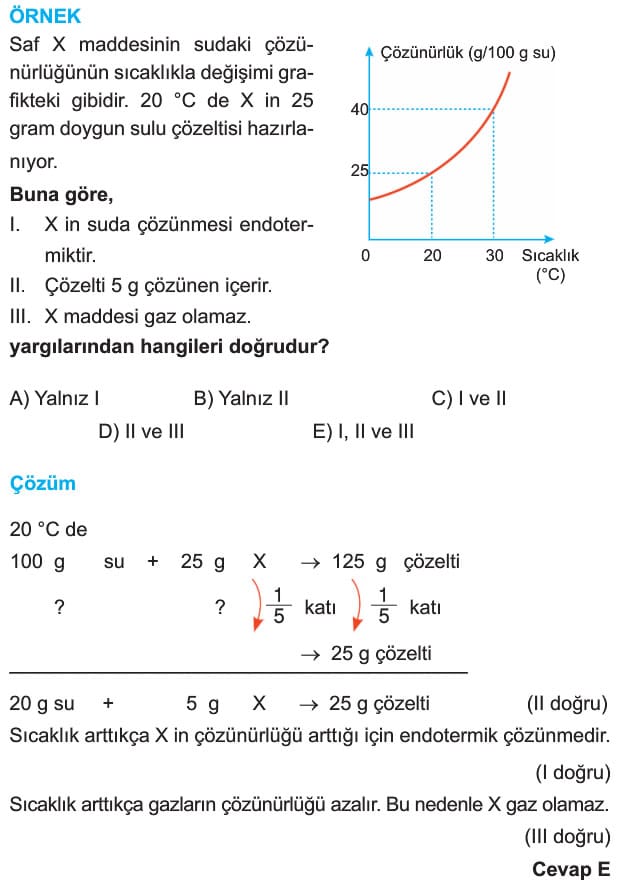
2. Sıcaklık
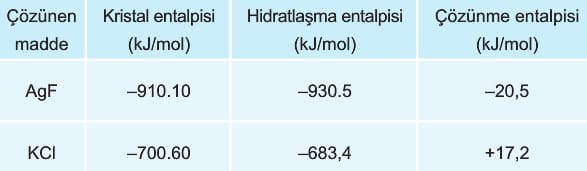
Çözünme olayının gerçekleşebilmesi için çözünen taneciklerin birbirinden ayrılması gerekir. Bu enerjiye kristal enerjisi denir. Aynı zamanda kristalden ayrılan tanecikler ile su arasında bir etkileşim olur ve bu enerjiye de hidratlaşma enerjisi denir.
Yukarıdaki örneklere bakıldığında AgF çözünmesi ekzotermik KCl nin çözünmesi endotermiktir. Bir başka ifadeyle suyun sıcaklığı azaldıkça AgF nin çözünürlüğü artarken, suyun sıcaklığı arttıkça KCl nin çözünürlüğü artar.
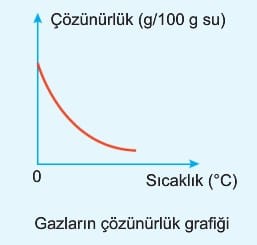
Saf katı ve sıvıların çözünmesi endotermik veya ekzotermik olabilirken gazların suda çözünmesi ekzotermiktir. Çünkü gaz molekülleri arasında çekim yok denecek kadar azdır.
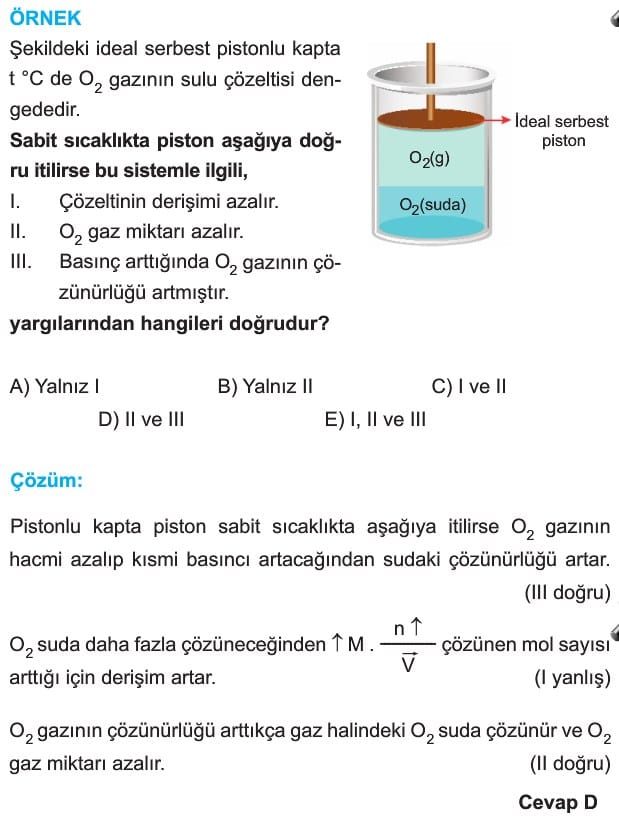
3. Basıncın çözünürlüğe Etkisi
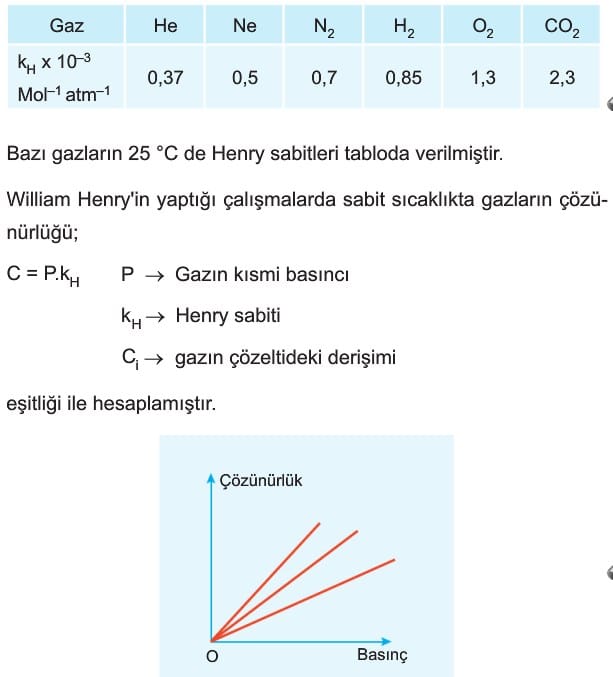
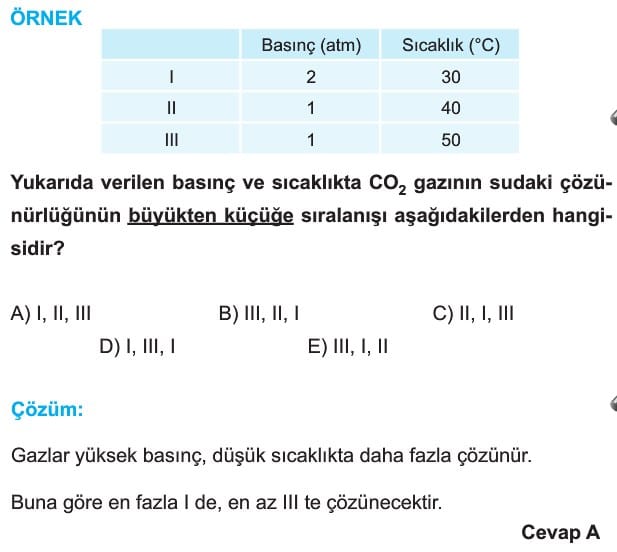
Katı ve sıvılarda basıncın çözünürlüğe etkisi yoktur. Gazların sudaki çözünürlüğünde, çözünmek istenen gazın kısmı basıncı önemlidir. Çözünmek istenen gazın kısmi basıncı arttıkça gazların çözünürlüğü de artar. Gazların çözünürlüğüne basıncın etkisini günlük hayatta birçok olayda gözlemleyebiliriz.
Maden suyu, gazoz gibi gazlı içeceklerin kapakları açıldığında gaz çıkışı meydana gelir. Bunun nedeni kapak açıldığında gaz basıncı azalır ve suyun içinde çözünmüş olan gazın bir kısmı dışarıya çıkar. Dalgıçlar, denizin diplerine indikçe basınç artması nedeniyle kandaki gaz çözünürlüğü artar, hızlı bir şekilde su yüzeyine çıkıldığında dış basınçta ani düşüş; kanda çözünmüş olan gazın dışarı çıkmasına neden olur. Bu gaz damarlara basınç yaparak damarların patlamasına neden olur.
Aynı durumu dağcılarda görebiliriz. Yükseklere çıkıldıkça atmosfer basıncı azalır. Bu durumda vücut içi basıncı daha fazla olur ve kılcal damarların çatlaması, kulaklarımızda basınç artış hissi gözlenir.
Bu kanun, ancak seyreltik çözeltilerde uygulanabilir. NH3, NO2, SO2 gibi gazlar suda kimyasal tepkimeyle çözündükleri için bu kanun uygulanmaz.
4. Ortak İyon Etkisi
Çözünmek istenen maddenin içindeki iyonlardan çözelti içerisinde varsa çözünme saf sudakinden az olacaktır. Ortak iyon derişimi ne kadar fazla ise çözünme o kadar azdır. Ortak iyon etkisi çözeltilerde denge ünitesinde ayrıca işleyeceğiz. Eğer ortak iyon yoksa çözünme saf sudakine eşittir.
Farklı Çözeltilerin Karıştırılması İle Oluşan Yeni Çözeltilerde Derişim
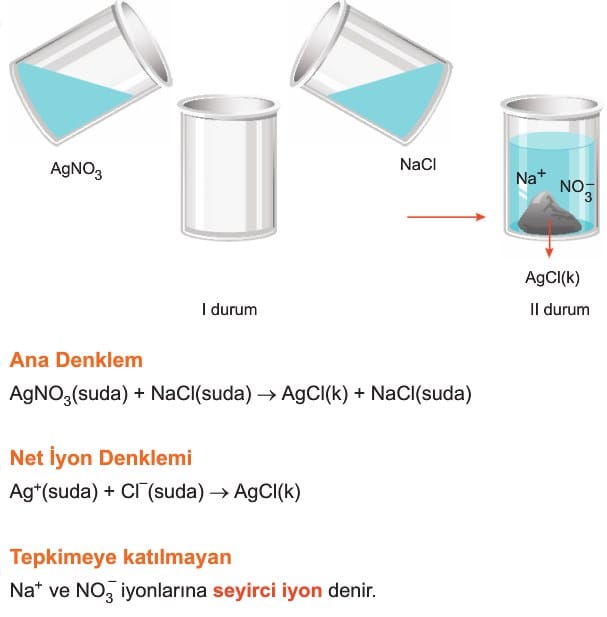
Özellikle iki farklı çözelti karıştırıldığında iyonlar yeniden düzenlenerek suda çözünmeyen katı oluşturabilirler veya bir çözelti içerisine başka bir element veya bileşik eklenerek ortamda farklı iyonlar oluşturabilirler. Bu durumda maddelerin derişimi hesaplanırken maddenin mol sayılarındaki ve çözelti hacmindeki değişime dikkat edilmelidir.
Örneğin AgNO3 çözeltisi ile NaCl çözeltileri karıştırıldığında ortamdaki Ag+ ve Cl– iyonları suda çok az çözünen veya çözünmüyor kabul edebileceğimiz AgCl katısı oluşturabilirler. Bu durumda ortamda Na+, NO3– derişimleri ile birlikte eğer artan Ag+ ve Cl– iyonlarından birinin derişimi hesaplanabilir.
Çözünürlüğe Etki Eden Faktörler Soruları ve Çözümleri
Çözümlü Örnek Test Soruları
Çözünürlüğe Etki Eden Faktörler
Çözünürlük, sadece sıcaklık ve basınca değil, aynı zamanda çözücü ve çözünenin kimyasal yapısı gibi birçok faktöre bağlıdır. Ayrıca, çözünürlüğe gazlar için basınç da önemli bir etki yapar.
1. Bir gazın su içerisindeki çözünürlüğü sıcaklık arttıkça nasıl değişir ve bu durumu hangi yasa açıklar?
A) Çözünürlük artar, Boyle yasası ile açıklanır.
B) Çözünürlük azalır, Henry yasası ile açıklanır.
C) Çözünürlük artar, Henry yasası ile açıklanır.
D) Çözünürlük azalır, Dalton yasası ile açıklanır.
Çözüm: Gazların çözünürlüğü sıcaklık arttıkça genellikle azalır ve bu durum Henry yasası ile açıklanır. Cevap B.
2. Doymuş bir çözeltiye, çözünen miktarı artırıldığında ne olur ve bu durumu hangi faktörler etkiler?
A) Çözelti daha doygun hale gelir ve çözünen dibe çöker, sıcaklık önemli rol oynar.
B) Çözünme devam eder, çünkü çözelti doygun hale gelemez.
C) Çözelti sabit kalır, basınç önemli bir rol oynar.
D) Çözünen tamamen çözülür, çözelti doygun hale gelir.
Çözüm: Doymuş bir çözeltiye daha fazla çözünen eklenirse, çözünme durur ve çözünen fazlalığı dibe çöker. Sıcaklık çözünürlüğü etkileyen önemli bir faktördür. Cevap A.
3. Aşağıdaki maddelerden hangisinin su içerisindeki çözünürlüğü sıcaklık arttıkça azalır?
A) Şeker
B) Tuz
C) Karbondioksit
D) Sodyum hidroksit
Çözüm: Gazlar, sıcaklık arttıkça çözünürlüğü azalan maddelerdir. Karbondioksit bir gaz olduğu için sıcaklık arttıkça su içinde çözünürlüğü azalır. Cevap C.
4. Yüksek basınç altında bir gazın sıvı içindeki çözünürlüğü hakkında aşağıdaki ifadelerden hangisi doğrudur?
A) Çözünürlük azalır.
B) Çözünürlük artar.
C) Çözünürlük sabit kalır.
D) Çözünürlük basınçla değişmez.
Çözüm: Henry yasasına göre, gazların çözünürlüğü basınç arttıkça artar. Yüksek basınç altında gazların sıvılar içindeki çözünürlüğü artar. Cevap B.
5. Bir çözücünün içerisinde çözünmüş madde miktarının artırılması çözeltinin hangi özelliğini değiştirebilir?
A) Yoğunluğunu artırır.
B) Sıcaklığını artırır.
C) Rengini değiştirir.
D) Sadece hacmini artırır.
Çözüm: Çözücünün içerisinde çözünmüş madde miktarı arttıkça çözeltinin yoğunluğu da artar. Cevap A.
6. Aşağıdakilerden hangisi katıların çözünürlüğünü artıran bir faktördür?
A) Basıncın düşürülmesi
B) Sıcaklığın artırılması
C) Çözünen madde miktarının azaltılması
D) Gaz ilave edilmesi
Çözüm: Katıların çözünürlüğü genellikle sıcaklık arttıkça artar. Cevap B.